Blog
Titulación: fin del análisis de proteínas Kjeldahl
titulacion,análisis,proteínas,kjeldahl
La titulación es una de las técnicas más utilizadas en los laboratorios, sin embargo, algunos detalles garantizan su eficacia, pudiendo evitar errores en la determinación de la concentración de proteína en la muestra.
La titulación es el último paso del análisis de proteínas por el método Kjeldahl y ocurre después del muestreo y preparación de las muestras.
El método de determinación de nitrógeno total fue desarrollado hace más de 130 años por el danés Johan Gustav Kjeldahl y desde entonces ha sido estudiado, modificado y mejorado. El método Kjeldahl es una referencia o estándar para cuantificar el contenido proteico en los alimentos, siendo recomendado por organismos estandarizadores como AOAC e ISO. Este método cuantifica el contenido de nitrógeno total y estima indirectamente el contenido proteico de los alimentos.
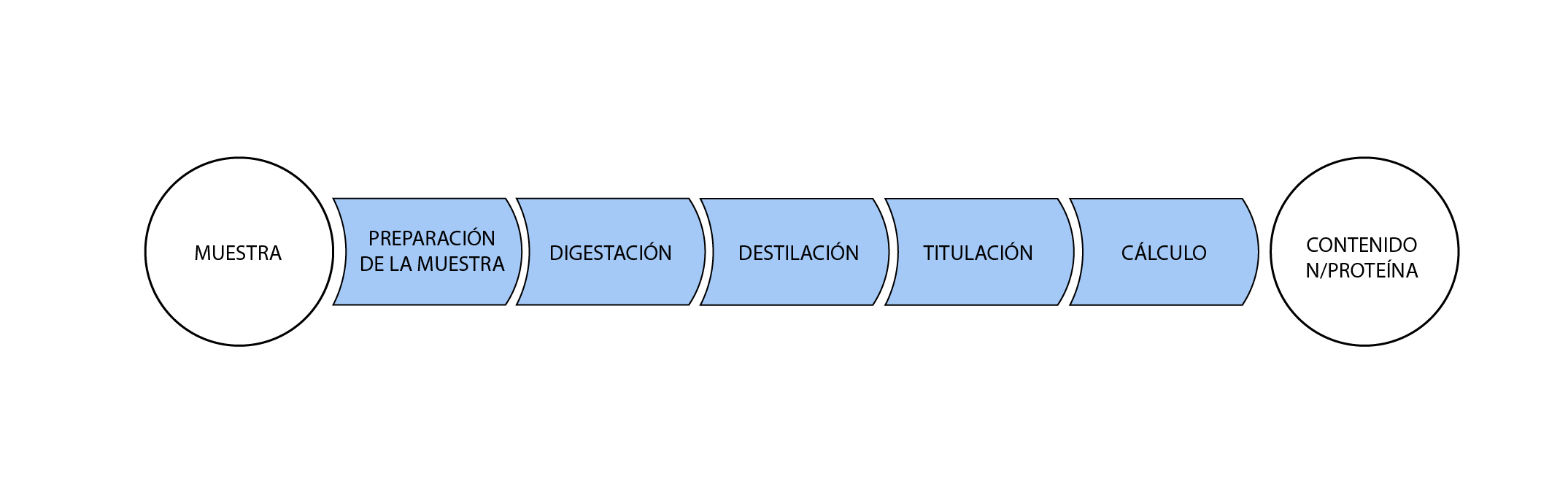
Método Kjeldahl
El
método consiste en la
El último paso es la titulación con ácido fuerte estandarizado para cuantificar el nitrógeno total presente en la muestra. Luego, el contenido de proteína se estima indirectamente a través del cálculo multiplicando el contenido de nitrógeno por un factor de conversión.
El
resultado final del análisis, es decir, el contenido
de proteínas, depende de la calidad de cada paso del proceso analítico.
Titulación
La titulación es un análisis químico cuantitativo utilizado para determinar la concentración de una sustancia en una muestra. El principio básico de la titulación es agregar un titulador o una solución estándar de concentración conocida a la solución que se va a analizar.
La
solución titulante se agrega lentamente con la ayuda de una
En
el análisis de proteínas, el destilado obtenido en el paso anterior se somete a
titulación. El amoníaco se titula directamente con ácido clorhídrico
estandarizado (HCl 0,1 mol/L) que desplaza la molécula de borato, separando el
borato de amonio formado en la
El volumen de solución titulante requerido para la muestra y para la muestra en blanco, junto con el factor de corrección de ácido clorhídrico y el factor de conversión de nitrógeno se utilizan para el cálculo final para obtener la concentración de proteína en la muestra (cálculo disponible al final de la página). El factor de conversión de nitrógeno varía según el tipo de producto, pero en general se aplica un valor de 6,25 para varias muestras.
Aunque todos los pasos del análisis de proteínas deben realizarse con prudencia, la no estandarización o la estandarización incorrecta del ácido clorhídrico es la mayor fuente de errores en el paso de titulación. Además, la definición del punto de parada de la titulación también afecta el resultado del análisis.
Estandarización del ácido
La estandarización de las soluciones juega un papel clave en los métodos de análisis titulométricos. En una estandarización, la concentración de una solución volumétrica se determina por su titulación frente a una cantidad cuidadosamente medida de un estándar primario, un estándar secundario o el volumen exactamente conocido de otra solución estándar.
Este
procedimiento es muy común en el laboratorio para definir la concentración
exacta de una solución preparada con un constituyente (soluto) volátil,
higroscópico o poco puro.
La
no estandarización o estandarización incorrecta del ácido clorhídrico puede
comprometer todos los pasos anteriores (
Punto final da titulación
El punto final de la reacción se determina comprobando un cambio en una propiedad física, como el color, para tratar de determinar el punto de equivalencia. Este punto se puede determinar visualmente, utilizando indicadores.
Los indicadores no cambian de color al instante. En el caso de la titulación ácido-base, el indicador puede ser inicialmente de color más claro antes de cambiar por completo. En el análisis de proteínas, la solución destilada se titula con ácido clorhídrico estandarizado 0,1 mol/L, hasta la aparición de un color ligeramente rojizo y persistente, como se muestra en la siguiente figura.

Cada
analista puede percibir los colores de manera diferente, lo que puede afectar
la precisión y repetibilidad del resultado. Si el color cambia poco, se agrega
una gran cantidad de titrante, lo que perjudica los resultados finales. De esta
forma, la experiencia y percepción del analista contribuyen a
la estandarización de los resultados.
Consideraciones finales
Un error de laboratorio es cualquier falla que ocurra en cualquier parte del proceso de análisis. De esta forma, un laboratorio de análisis necesita disponer de un control de calidad que permita comprobar que los procedimientos se están realizando correctamente.
Crear una lista de los principales errores y cómo cada uno puede afectar el resultado es una herramienta útil para usar.
Además, es de suma importancia que los procedimientos sean realizados por un equipo capacitado y calificado, ya que la falta de preparación se considera una interferencia, no solo para el análisis de proteínas, sino también para otros procesos.
Es importante que el equipo utilizado esté en perfectas condiciones y la cristalería utilizada debe estar calibrada.
El proceso de muestreo, que incluye la recolección de muestras, el cuarteo, la homogeneización y la molienda, es tan importante como los pasos de digestión, destilación y titulación.
En
la preparación de soluciones y desarrollo del proceso analítico se debe
utilizar agua de buena calidad, ya que también se considera un interferente.
Obtenga más información en el contenido sobre "Tipos de agua utilizados en el laboratório y sus principales aplicaciones".
1) Solución volumétrica estandarizada de Ácido clorhídrico 0,1 mol/l
Medir 8,5 mL de ácido clorhídrico y transferir a un matraz aforado de 1000 mL, que contenga aproximadamente 500 mL de agua. Enfriar, completar el volumen y homogeneizar.
Estandarización: pesar aproximadamente 0,133 g de carbonato de sodio en un matraz Erlenmeyer, previamente secado a 105°C durante 2 horas. Disolver en 50 ml de agua. Añadir 3 gotas de solución de rojo de metilo al 0,1 % (p/v). Titular hasta tornarse rosa. Calentar hasta ebullición para eliminar el dióxido de carbono. Si el color rosa no es persistente, enfríe y continúe con la titulación. El punto exacto de inflexión de la solución de ácido clorhídrico de 0,1 mol/L se produce a un pH de 4,4.
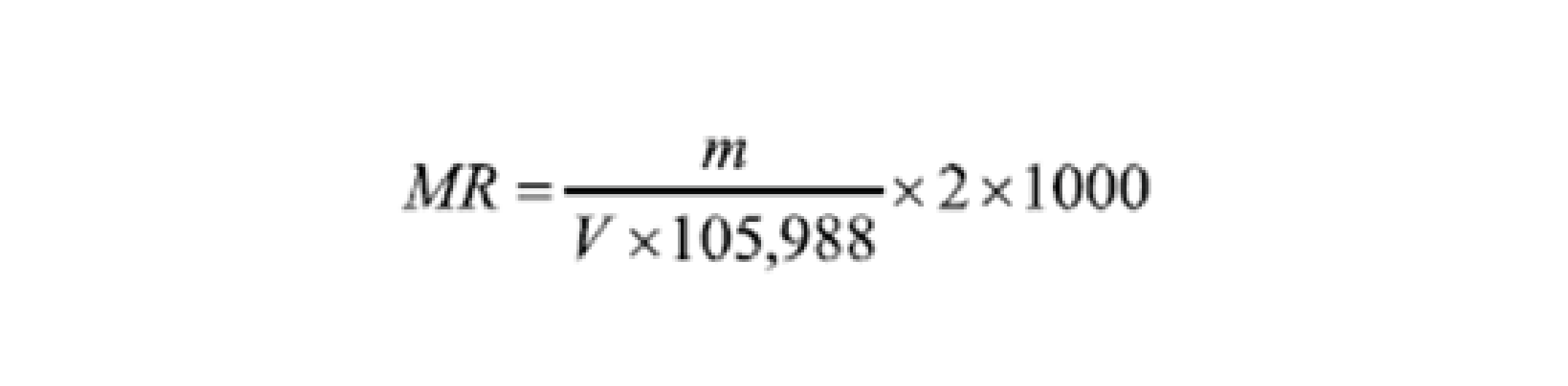
Donde:
MR: molaridad real de una solución de ácido
clorhídrico de 0,1 mol/L.
M: Masa de carbonato de sodio, en g.
105.988: Masa molar de carbonato de sodio.
V: Volumen de solución de ácido clorhídrico 0,1 mol/L
utilizado en la titulación, en mL.
2/1: Relación estequiométrica entre el ácido
clorhídrico y el carbonato de sodio.
2) Cálculo final
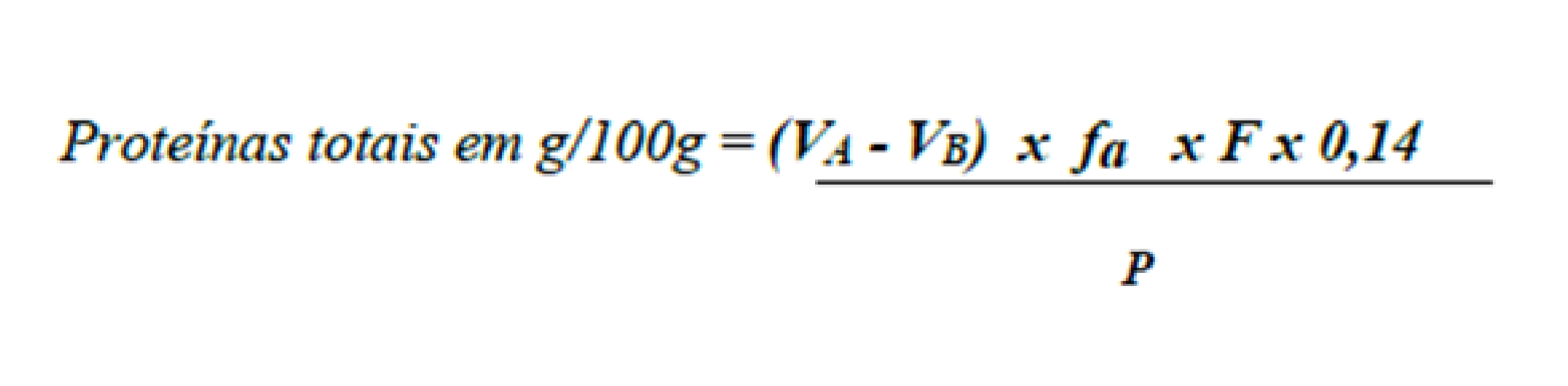
VA = volumen de ácido clorhídrico estandarizado de 0,1
mol/L gastado en la titulación de la muestra.
VB = volumen de ácido clorhídrico estandarizado de 0,1
mol/L gastado en la titulación en blanco.
fa = factor de corrección de 0,1 mol/L de solución de
ácido clorhídrico.
F = factor de conversión de nitrógeno a
proteína. En la mayoría de los alimentos se estima que el nitrógeno representa
aproximadamente el 16% del peso de proteína, por lo que en 100g de proteína hay
16g de nitrógeno, y 100/16= 6,25, que corresponde al factor de conversión de
nitrógeno para proteína. A continuación se presentan algunos factores de
conversión sugeridos.

Si quiere saber más, descargue el e-book exclusivo.
Sobre a Tecnal
Tecnal tiene como misión contribuir para el desarrollo científico, tecnológico y con la industria nacional e internacional por medio de la fabricación y comercialización de equipos científicos, de la prestación de servicios especializados, y de la difusión del conocimiento. La empresa busca crecer de manera innovadora y sustentable, enfocada en la continuidad y excelencia operacional, de forma a convertirse en una referencia en el mercado brasileño e internacional de equipos científicos. Comuníquese con nosotros: teléfono/WhatsApp +55 (19) 997441017, e-mail: comex@tecnal.com.br o por nuestra página web haciendo clic aquí.
Referencias
IAL,
Instituto Adolfo Lutz. Métodos físico-químicos para análise de alimentos. São
Paulo: Instituto Adolfo Lutz, p. 1020, 2008.
LOCATELLI,
Tamiris. Determinação de proteínas em suplementos alimentares. Revista
Cientifica Multidisciplinar Núcleo do Conhecimento. Ano 03, Ed 08, Vol. 03, pp
21-47, Agosto 2018. ISSN:2448-0959
SINDIRAÇÕES, Sindicato Nacional da Indústria de Alimentação Animal. Compêndio Brasileiro de Alimentação Animal. Guia de métodos analíticos. 2017




