Blog
Análisis de laboratorio de carbohidratos
analisis,laboratorio,carbohidratos
Los
análisis de carbohidratos, como el método de Fehling, ofrecen información
importante sobre la presencia y cantidad de estos compuestos en las muestras,
lo que permite una evaluación precisa de su composición.
La macromolécula más abundante que se encuentra
en la naturaleza son los carbohidratos. Desempeña un papel esencial en la
biología y la nutrición y es una de las principales fuentes de energía de los
seres vivos. Para comprender su estructura, composición y función son
necesarios análisis específicos de laboratorio. En este texto exploraremos la
definición, composición, funciones y métodos para determinar los carbohidratos,
centrándonos en el método Lane-Eynon.
¿QUÉ SON LOS CARBOHIDRATOS?
Los carbohidratos son biomoléculas que
constituyen los seres vivos, así como los ácidos nucleicos, las proteínas y los
lípidos. Se les conoce como hidratos de carbono, azúcares o glucídios, además
de ser fuentes de energía, también son fundamentales en diversos procesos
biológicos.
Están compuestos por átomos de carbono (C),
hidrógeno (H) y oxígeno (O), en proporción 1:2:1, representados por la fórmula
general CH2O, su estructura química básica está formada por cadenas
o anillos formados por unidades de monosacáridos, que son los componentes
básicos de los carbohidratos. Algunos carbohidratos pueden tener otro tipo de
átomos en sus moléculas, como ocurre con la quitina, que tiene átomos de
nitrógeno.
Existen tres clases principales de
carbohidratos, monosacáridos, disacáridos y polisacáridos, que se dividirán según
la cantidad de átomos de carbono en sus moléculas. Veremos más detalles a
continuación.
MONOSACÁRIDOS: LOS CARBOHIDRATOS SIMPLES
Los monosacáridos, o azúcares simples, son los
carbohidratos más simples, de los que derivan todas las demás clases. Están
formados por una única molécula de azúcar, de tres a siete átomos de carbono,
generalmente en forma de cadena o anillo.
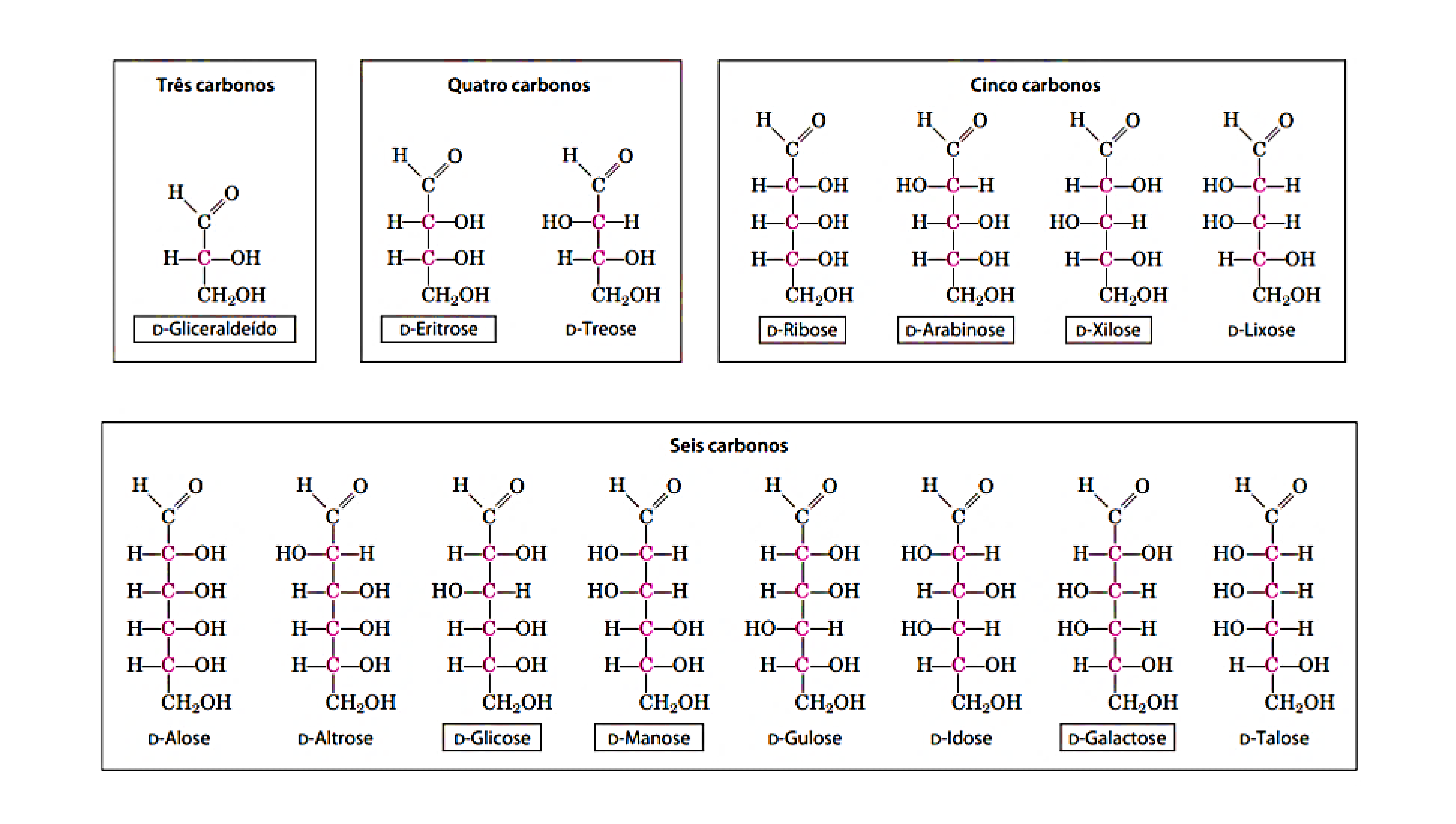
Figura
01.
Monosacáridos tipo aldosa. Fuente: Rafael Salomão da Silva, 2022.
Los monosacáridos más comunes son la glucosa,
la fructosa y la galactosa. La glucosa se caracteriza por ser la principal
fuente de energía del cuerpo humano, se puede encontrar en una amplia variedad
de alimentos, como cereales, verduras y frutas. La fructosa se encuentra en las
frutas y la miel, y la galactosa no es tan común, estando presente en los
productos lácteos y otros productos alimenticios.
Entre las funciones de los monosacáridos se
encuentra la síntesis de otras sustancias, como ácidos nucleicos,
glicoproteínas y glicolípidos, además de ser utilizados en la síntesis de
glucógeno (almacenamiento de energía en animales) y almidón (almacenamiento de
energía en plantas).
¿Y ha oído hablar de los disacáridos? Se
diferencian porque están compuestos por dos moléculas de monosacáridos.
DISACÁRIDOS: ENLACE DE DOS MOLÉCULAS DE
AZÚCAR
Los disacáridos son carbohidratos formados por
la unión de dos monosacáridos, mediante un enlace glicosídico, que se produce
durante el proceso de deshidratación, liberándose una molécula de agua.
La sacarosa es uno de los disacáridos más
conocidos, presente en el azúcar de mesa, y está compuesta por una molécula de
glucosa y una molécula de fructosa, y se encuentra en alimentos dulces,
gaseosas, azúcar de caña y azúcar refinada. Son importantes fuentes rápidas de
energía en la dieta humana, el cuerpo humano las metaboliza fácilmente y
desempeñan varias funciones biológicas esenciales.
La lactosa es otro disacárido importante, que
se encuentra en la leche y sus derivados, siendo la principal fuente de
carbohidratos en la leche materna, está compuesta por una molécula de glucosa y
una molécula de galactosa y requiere de la presencia de la enzima lactasa para
ser digerida y absorbida por el organismo. . Las personas tienen intolerancia a
la lactosa debido a la baja producción de lactasa.
Además de la sacarosa y la lactosa, existen
otros disacáridos, como la maltosa, que está formada por dos moléculas de
glucosa, y la trehalosa, que está formada por una molécula de glucosa y una
molécula de fructosa. También son importantes fuentes de energía en la dieta
humana y están presentes en cereales, tubérculos y algunas frutas.
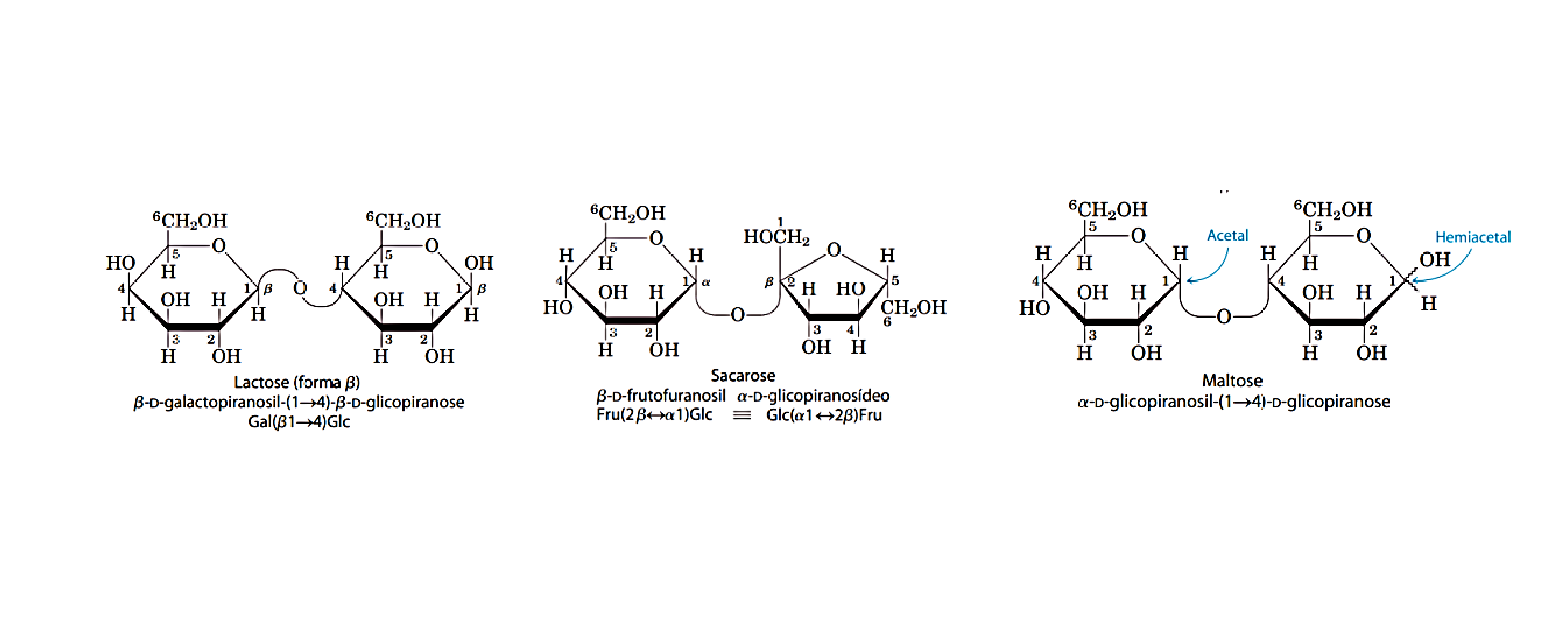
Figura
02.
Los principales polisacáridos: lactosa, sacarosa y maltosa. Fuente: Rafael
Salomão da Silva, 2022.
POLISACÁRIDOS: CARBOHIDRATOS COMPLEJOS
Los polisacáridos o glicanos son macromoléculas
formadas por la unión de muchas unidades de monosacáridos, conectadas mediante
enlaces glicosídicos, son carbohidratos complejos. Los polisacáridos más
importantes son el almidón, el glucógeno y la celulosa.
El almidón está formado por moléculas de
glucosa unidas entre sí y es uno de los polisacáridos más abundantes en la
naturaleza, se encuentra en las plantas y actúa como reserva de energía. Cuando
se consume aporta energía a los organismos porque en el proceso digestivo se
descompone en moléculas de glucosa.
La celulosa es un componente estructural que se
encuentra en las paredes celulares de las plantas, que proporciona rigidez y
resistencia a las estructuras de las plantas, lo cual es crucial para mantener
la estructura y el soporte de las plantas. Al igual que el almidón, también es
un polímero de glucosa, pero con enlaces tipo b, que forman fibras insolubles
en agua que no son digeridas por los humanos.
Otro polisacárido importante es el glucógeno,
encargado de ser reserva de la célula animal, almacenado en el hígado y
músculos y utilizado como fuente rápida de glucosa. Similar al almidón, pero
con mayor número de enlaces. Los polisacáridos, en resumen, desempeñan varias
funciones biológicas, desde el almacenamiento de energía, el soporte
estructural y el suministro de sustratos metabólicos.
MÉTODOS DE ANÁLISIS DE LABORATORIO EN
CARBOHIDRATOS
Existen varios métodos utilizados para analizar
los carbohidratos (azúcares), entre los más comunes se encuentran la
cromatografía, la espectroscopia y la titulación. Veamos a continuación:
CROMATOGRAFIA
La cromatografía
es una técnica que separa los componentes de una mezcla en función de sus
propiedades de interacción con una fase estacionaria y una fase móvil. En la
cromatografía líquida de alta resolución (HPLC), la fase móvil (solvente
líquido) se bombea a través de una columna, mientras que la fase estacionaria
(resina porosa o partículas recubiertas) retiene los componentes de la muestra.
A medida que la fase móvil fluye a través de la columna, los componentes quedan
atrapados y separados por la fase estacionaria, lo que permite la detección.
Con la cromatografía de gases (GC), los
carbohidratos se convierten en derivados volátiles antes del análisis. La
muestra se inyecta en un inyector calentado, se vaporiza y se inyecta en la
columna cromatográfica. Dentro de la columna, los componentes de la muestra se
separan en función de sus interacciones con la fase estacionaria y
posteriormente se detectan.
ESPECTROSCOPIA
La espectroscopia consiste en medir la
interacción de la luz con la muestra, lo que permite cuantificar sustancias en
función de la absorción o transmisión de luz en diferentes longitudes de onda.
En el análisis de carbohidratos, este método aprovecha las propiedades
específicas de absorción de luz de ciertos grupos funcionales que se encuentran
en las moléculas.
Para el análisis, la muestra con carbohidratos
debe prepararse y diluirse según la metodología elegida. Posteriormente, la
muestra se mide en un espectrofotómetro a una serie de longitudes de onda
específicas, la luz pasa a través de la muestra y el espectrofotómetro registra
la cantidad de luz absorbida por los carbohidratos presentes. La absorbancia
registrada se compara con una curva estándar construida previamente utilizando
soluciones estándar de carbohidratos en concentraciones conocidas.
TITULACIÓN
La titulación es el método clásico que implica
la adición gradual de un reactivo de concentración conocida a una muestra hasta
que ocurre la reacción química específica. Estos métodos son esenciales para
determinar la cantidad, composición y propiedades de los carbohidratos en una
variedad de muestras, desde alimentos y bebidas hasta productos farmacéuticos y
biomateriales. La elección del método más adecuado depende de las
características específicas de la muestra y de los objetivos del análisis.
En la titulación redox utilizando un indicador
colorimétrico, la muestra que contiene el carbohidrato de interés se agrega al
reactivo mantenido en ebullición hasta que se produce un cambio de color, lo
que indica el punto final de la reacción. Este método se utiliza a menudo para
determinar los carbohidratos reductores, como la glucosa, utilizando soluciones
de Fehling o Benedict.
A la hora de valorar azúcares reductores se
suele utilizar el método de Lane-Eynon (Fehling); veremos más detalles de este
método a continuación.
MÉTODO LANE-EYNON
El método Lane-Eynon, también conocido como
método de Fehling, es una técnica analítica utilizada para determinar la
presencia de azúcares reductores en una muestra determinada, y se utiliza en
laboratorios de alimentos, bebidas y bioquímica.
Este método implica el uso de dos soluciones,
llamadas solución A de Fehling y solución B de Fehling. La solución A es
sulfato de cobre (II) en un medio ácido, mientras que la solución B es una
solución alcalina de tartrato de potasio e hidróxido de sodio. Estas soluciones
deben prepararse por separado y conservarse en frascos oscuros, ya que son
sensibles a la luz.
Tradicionalmente, este análisis de titulación
requiere el uso de un mechero Bunsen o una placa caliente, lo que hace que el
procedimiento sea más lento, más peligroso y menos preciso, debido a la
dificultad para estandarizar la temperatura.
La prueba de Fehling consiste en agregar a la
muestra la solución A de Fehling y calentarla para oxidar el carbohidrato,
reduciendo el ion cúprico, para formar óxido de cobre (I) insoluble, de color
rojo o naranja. A continuación se añade solución B de Fehling, formando un
complejo azul de ion cobre (II) y tartrato que indica la presencia de azúcares
reductores. La intensidad del color está relacionada con la concentración de
carbohidratos, lo que permite la determinación semicuantitativa de la
concentración de carbohidratos.
Para comprobar la finalización del proceso se
puede utilizar azul de metileno, cuya forma reducida es incolora. Sin embargo,
es importante que el proceso no exceda los 3 minutos, ya que cualquier tiempo
más allá de esto resultará en la descomposición de los azúcares y del propio
azul de metileno, especialmente durante el calentamiento prolongado entre 105 y
110°C.
Para optimizar el procedimiento, Tecnal
desarrolló el Determinador de Azúcar
Reductor, modelos TE-0861 y TE-088, basado en el método Lane-Eynon.
El uso de este equipo elimina la necesidad de accesorios adicionales, como un
mechero Bunsen, lo que se traduce en una mayor seguridad a la hora de realizar
los análisis, y el calentamiento con vapor facilita un intercambio de calor más
uniforme.
El modelo TE-088 cuenta con un electrodo de
platino, que reemplaza al azul de metileno para indicar el punto final de la
titulación, esto garantiza la precisión del método, en comparación con el
método tradicional, por lo que el punto de inflexión se puede visualizar
mediante escala numérica, independientemente. sobre el cambio de color de la
solución.
Para utilizar este equipo se requiere que el
extracto esté listo para la titulación y para determinar los azúcares totales
se debe realizar primero una hidrólisis ácida. Previamente se debe calentar el
determinador de azúcar reductor, luego se agregan las soluciones de Fehling al
tanque, completando con agua hasta cubrir el electrodo. Posteriormente se
activa el potenciómetro, y cuando se completa la ebullición de las soluciones
se debe iniciar la titulación de la muestra en la bureta.
Otros equipos que se pueden utilizar en este
proceso: balanza de precisión, balanza analítica, desecador, destilador de
agua, medidor de pH y baño maría.
¿Quiere saber más? ¡Descarga el e-book
exclusivo sobre “Azúcares reductores” elaborado por Tecnal! En éste encontrará
definición, importancia, métodos de determinación, cómo se realiza el análisis
y sus ventajas.
CONSIDERACIONES FINALES
A lo largo de este texto vimos la definición,
funciones, tipos de carbohidratos y los métodos utilizados en su determinación.
Métodos como la cromatografía, la espectroscopia, la titulación y el método
Fehling (Lane-Eynon) son herramientas valiosas para la industria y la
investigación, ya que permiten análisis precisos y confiables de carbohidratos
en diversas muestras.
Por lo tanto, comprender las técnicas de
análisis de laboratorio de carbohidratos es fundamental para garantizar la
calidad y seguridad de los productos que consumimos y utilizamos en nuestra
vida diaria y para las investigaciones en el área.
REFERENCIAS
BIBLIOGRÁFICAS
CAÑIZARES, G. I. L.; RODRIGUES, L.; CAÑIZARES,
M. C. Metabolismo de carboidratos não-estruturais em ruminantes. Archives of veterinary Science, p.
63-73, 2009.
CORSINO, J. Bioquímica - Campo Grande, MS: Ed. UFMS, 213 p. 2009.
GARDIN, J. P. P. et al. Metodologia de
determinação de açúcares solúveis em tecido vegetal de cafeeiro por
cromatografia gasosa. Simpósio de
Pesquisa dos Cafés do Brasil, 2005.
MARQUES, M. R. F. Bioquímica, 1. ed. Revisada - Florianópolis: BIOLOGIA/EAD/UFSC,
2014.
MATOS FILHO, H. A.; CARVALHO, R. de C. M.
Análise de carboidratos solúveis em plantas de arroz. Científic@-Multidisciplinary Journal, v. 7, n. 1, p. 1-8, 2020.
PAULI, E. D.; CRISTIANO, V.; NIXDORF, S. L.
Método para determinação de carboidratos empregado na triagem de adulterações
em café. Química Nova, v. 34, p.
689-694, 2011.
TECNAL. Açucares
redutores. Piracicaba: Tecnal, p. 12, E-book. 2022.





